국내 연구팀이 간암 억제 유전자 HDAC6 조절을 통한 간암세포 억제 효과와 종양 면역 활성화 기전을 찾았다.
가톨릭의대 병리학교실 남석우 교수팀은 ‘HDAC6→Let-7i-5p→TSP1→CD47’ 조절 기전 제어에 의해 간암 발생이 억제되는 것을 확인했다고 밝혔다.
HDAC6는 히스톤 탈아세틸화 효소의 하나로, 간암 억제 유전자로서 치료적 가능성은 인정된 바 있다.
남석우 교수팀은 HDAC6가 대표적인 후성유전조절인자 중 하나라는 사실에 근거하여, 정상 간세포에서 암 발생에 기여하는 다양한 마이크로 RNA(microRNAs)를 제어할 것이라는 가설을 세웠다.
이러한 과정을 통해 연구팀은 간암 발생 과정에서 HDAC6가 그 기능을 소실하거나 억제되었을 때 특이적으로 증가하는 종양 유발 마이크로 RNA를 탐색한 결과 Let-7i-5p를 특정할 수 있었다.
연구팀은 Let-7i-5p가 생체 내 강력한 혈관 신생 및 종양 성장 억제제로 잘 알려진 트롬보스폰딘-1(Thrombospondin-1, TSP1)의 단백질 번역을 저해함으로써 간암 생성에 기여한다는 사실을 규명하였다.
또한, Let-7i-5p에 의해 억제된 트롬보스폰딘-1은 대식세포의 종양세포 포식작용(phagocytosis)을 활성화하지 못해 종양 면역 기능 소실을 유발한다는 사실을 증명했다.
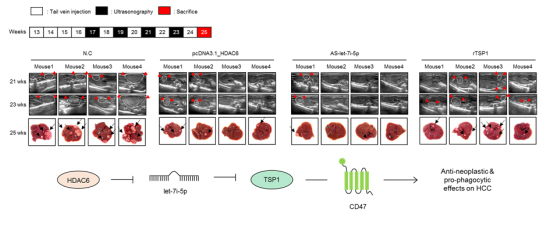
쥐를 이용한 동물실험 결과 HDAC6의 활성을 유발하면 종양 유발 마이크로 RNA인 Let-7i-5p의 생성이 억제되는 것을 관찰할 수 있었다.
Let-7i-5p의 생성이 억제됨에 따라 트롬보스폰딘-1의 단백질 생성 증가에 의해 종양세포 성장, 전이 및 혈관 신생화가 억제되는 것을 볼 수 있었다.
특히 최근 종양세포의 CD47 수용체와 대식세포의 면역억제 수용체인 SIRPa가 결합하여 종양 면역을 회피하는 것으로 알려져 있으나, 남 교수팀의 연구에서는 HDAC6에 의해 조절되는 트롬보스폰딘-1이 종양세포의 CD47 수용체와 우선적으로 결합함으로써 대식세포의 종양 면역 기전을 활성화 한다는 것을 세포주 및 동물실험 수준에서 확인할 수 있었다.
남석우 교수는 “이번 연구는 HDAC6를 간암 억제 유전자로 최초 보고한 후, 후속 연구를 통해 종양 미세환경에서 실제 종양세포와 면역세포 및 간세포의 복잡한 조절 네트워크를 규명한 것”이라며 “이를 통해 HDAC6-Let-7i-5p-TSP1 조절 축에 대한 특이적 제어를 이용한 간암 치료 가능성을 밝혀낸 최초의 연구 성과이며 새로운 간암 치료법의 초석이 될 것”이라고 밝혔다.
이번 연구 결과는 최근 세계적인 간질환 관련 학술지인 간학회지(Hepatology, IF 14.079) 게재되었으며, 논문은 생물학연구정보센터(BRIC)의 ‘한국을 빛내는 사람들’에 소개되었다.
















