‘의약품 수용체’로 불리는 G단백질 수용체 결합의 초기 구조가 규명돼 향후 신약 개발에 새로운 전략을 제시할 것이라는 주장이 제기됐다.
과학기술정보통신부는 성균관대 정가영 교수 연구팀이 G단백질수용체가 외부 신호와 결합해 세포 내 반응을 유도하기까지의 순차적인 구조 변화를 규명했으며, 나아가 약물 개발에 활용될 수 있는 G단백질수용체의 구조를 제시했다고 밝혔다.
G단백질수용체는 세포막의 문지기의 기능을 하며 호르몬, 의약품 등을 세포 내로 전달해 적절한 반응을 유도한다. 현재 사용 중인 의약품의 약 40%가 G단백질수용체를 통해 작용한다.
정가영 교수는 “지난 2012년 G단백질수용체 연구가 노벨화학상을 받은 이후로 이 수용체와 G단백질과 결합의 구조를 이용해 약물의 효과를 높이려는 시도가 많았지만 실질적인 결실은 없었다”고 말했다.
이에 연구팀은 G단백질수용체가 G단백질을 활성화시키는 과정을 연구한 끝에 결합 초기 G단백질수용체 구조가 세포 내 반응을 유도하는 효과적이라는 점을 밝혀냈다.
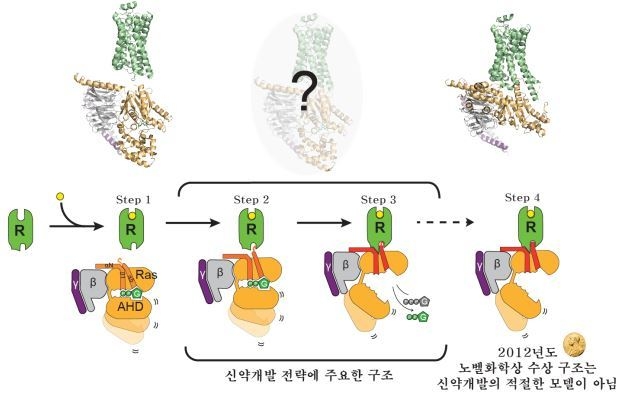
연구팀에 따르면, 그간 연구되어 온 G단백질수용체의 구조는 G단백질이 활성화된 이후의 형태(step4)로, G단백질 결합과정을 규명하기에 적절한 모델이 아니었다. 연구팀은 G단백질이 결합한 초기(step 2,3) 구조가 신약개발 추진에 더 적합하다고 덧붙였다.
정 교수는 “2012년 노벨화학상 이후 지속적으로 연구되어 온 G단백질수용체에 의한 G단백질 활성 원리의 패러다임을 바꾸는 이론을 제시했다”라며, “향후 G단백질수용체에 작용하는 의약품 개발의 새로운 전략이 될 것이다”라고 연구 의의를 설명했다.