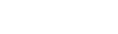국내 연구진이 대표적인 희귀 난치성 뇌질환인 ‘다계통 위축증(Multiple System Atrophy, MSA)’의 발병 기전을 규명하고, 잠재적 치료법을 제시했다.
 한국연구재단(이사장 홍원화)은 서울대학교 이승재 교수 연구팀이 톨유사수용체2(TLR2)*를 매개로 하는 다계통 위축증의 발병 기전을 규명하고, 이를 바탕으로 개발한 항체의 치료효과를 동물 모델에서 확인했다고 밝혔다.
한국연구재단(이사장 홍원화)은 서울대학교 이승재 교수 연구팀이 톨유사수용체2(TLR2)*를 매개로 하는 다계통 위축증의 발병 기전을 규명하고, 이를 바탕으로 개발한 항체의 치료효과를 동물 모델에서 확인했다고 밝혔다.
* 톨유사수용체2(TLR2): 인체 면역계에 존재하는 선천면역 수용체 중 하나로, 알파-시뉴클린 응집체를 인지하는 수용체로 알려져 있음
이번 연구 성과는 과학기술정보통신부와 한국연구재단이 추진하는 중견연구 사업 등의 지원으로 수행됐으며, 다학제 융합과학분야 국제학술지 ‘네이처 커뮤니케이션즈(Nature Communications)’에 1월 30일 게재됐다.
▲서울대학교 이승재 교수
다계통 위축증은 소뇌 및 기저핵의 신경퇴행을 동반하는 치명적 질환으로, 전 세계적인 고령화 추세에 따라 사회·경제적 문제로 대두됐다. 임상 증상이 비슷한 파킨슨병보다 진행 속도가 빠르고 예후가 불량해 환자의 삶의 질을 심각하게 저하시키지만, 현재 질병의 진행을 근본적으로 억제할 치료법이 부재한 실정이다.
이 질환은 알파-시뉴클린이 희소돌기아교세포 내에 축적돼 ‘교세포질내포함체(GCI)*’를 형성하는 것이 특징이다. 하지만 알파-시뉴클린의 발현량이 낮은 세포에 해당 단백질이 축적되는 경로가 아직 규명되지 않아 치료제 개발에 한계가 있었다.
* 교세포질내포함체(GCI, Glial Cytoplasmic Inclusion)는 주로 희소돌기아교세포(Oligodendrocyte)라는 뇌세포 안에 알파-시누클레인(α-synuclein)이라는 단백질이 비정상적으로 쌓여 만들어진 덩어리
이에 연구팀은 인간 줄기세포 및 마우스 모델을 활용해 알파-시뉴클린 응집체의 세포 간 전이 가설을 체계적으로 검증했다. 그 결과, 신경세포에서 생성된 응집체가 희소돌기아교세포로 흡수되어 환자 뇌 조직과 유사한 단백질 축적을 유도함을 확인했다.
연구진은 이 과정에서 단백질 알파-시뉴클린의 흡수를 매개하는 핵심 수용체인 ‘톨유사수용체2’에 주목했다. 분석 결과, 톨유사수용체2 매개 전이는 희소돌기아교세포의 성숙과 수초화(myelination)*에 필수적인 유전자 발현을 저해해 신경망 손상을 유발했다.
* 수초화: 뇌 신경세포 사이를 흐르는 전기신호가 빠르고 정확하게 전달되도록 신경 섬유(축삭)를 절연 물질로 감싸는 과정
실제 세포 및 동물 모델에서 톨유사수용체2 표적 단일클론항체* ‘NM-101’을 처리하자 단백질 축적이 현저히 감소했다. 또한 수초화 관련 유전자의 발현이 회복됐으며, 축삭** 손상과 운동 장애가 개선됨과 동시에 생존 기간이 연장되는 효과가 입증됐다.
* 단일클론항체: 하나의 표적(항원)만을 정밀하게 공격하도록 설계된 항체
** 축삭: 신경세포(뉴런)의 몸통에서 뻗어 나온 줄기 부분, 뇌와 우리 몸 전체에 전기신호를 전달하는 역할을 함
이번 연구는 병리 단백질 자체가 아닌 이를 매개하는 ‘수용체’를 차단함으로써, 구조적 이질성이 높은 단백질 응집체의 전이를 억제하는 새로운 치료 패러다임을 제시했다는 점에서 의의가 크다.
이승재 교수는 “이 전략은 다계통 위축증뿐만 아니라 파킨슨병 등 공통된 기전을 공유하는 다양한 시뉴클린병증* 치료를 위한 범용 플랫폼으로 확장될 것으로 기대된다”라며, “후속 연구를 통해 난치성 신경퇴행성 질환 치료제 개발을 앞당기겠다”라고 덧붙였다.
* 시뉴클린병증: 뇌 세포 내에 알파-시뉴클린 단백질이 비정상적으로 응집·축적되어 신경세포의 손상과 기능 저하를 초래하는 퇴행성 뇌질환을 통칭하는 용어
(그림1) 다계통 위축증 동물 모델에서 톨유사수용체2 항체에 의한 병리현상 조절 규명
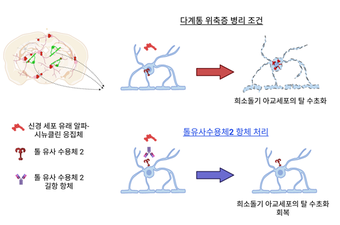
(그림2) 톨유사수용체2 항체에 의한 다계통 위축증 병리현상 조절 모델