폐암 환자에서 종양의 돌연변이를 분석해 항암제에 대한 약제내성을 대량으로 확인할 수 있는 기술이 개발됐다.
 연세대 의대 약리학교실 김형범 교수, 오형철 강사와 외과학교실 이승호 강사, 가톨릭대 의대 병리학교실 김영광 교수 연구팀은 차세대 유전자교정 기술인 프라임 편집기를 적용해 돌연변이 유발 및 검출 기술을 개발했으며, 이 기술을 통해 전체 돌연변이 중 95% 이상에서 약물 감수성 여부를 확인할 수 있다고 22일 밝혔다.
연세대 의대 약리학교실 김형범 교수, 오형철 강사와 외과학교실 이승호 강사, 가톨릭대 의대 병리학교실 김영광 교수 연구팀은 차세대 유전자교정 기술인 프라임 편집기를 적용해 돌연변이 유발 및 검출 기술을 개발했으며, 이 기술을 통해 전체 돌연변이 중 95% 이상에서 약물 감수성 여부를 확인할 수 있다고 22일 밝혔다.
이번 연구 결과는 국제학술지 ‘네이처 바이오테크놀로지(Nature Biotechnology, IF 33.1)’ 최신호에 게재됐다.
폐암 환자에서 표피생장인자수용체(EGFR) 변이는 전체 폐암 환자 중 30%에서 발견된다. EGFR 종양 돌연변이는 ‘티로신키나제 억제제(TKI)’와 같은 표적치료제의 사용 여부를 결정하는 중요한 기준으로 알려져 있다. 표적치료제는 치료 초기에는 좋은 반응을 보이나, 약물 사용 후 1~2년 후에는 새로운 돌연변이의 획득으로 발생하는 약제내성으로 인해 치료 효과가 감소하거나 재발하는 경우가 많다.
기존에는 약제내성과 돌연변이의 관계를 연구하기 위해 약제에 노출된 환자에서 종양 조직을 채취해 저항성 유전 변이를 발굴하는 방법을 사용했다. 하지만 환자마다 가진 돌연변이가 다르고 충분한 사례를 확보하기 어려워 단일 돌연변이 수준에서 약제내성을 평가하는데 어려움이 있었다.
연구팀은 EGFR 유전자의 대부분의 변이가 관찰되는 티로신키나제 영역에서 모든 형태의 돌연변이를 유도할 수 있는 차세대 유전자교정 기술인 프라임 편집기를 적용해 인공지능 기반의 돌연변이 검출 기술 ‘PEER-seq(Prime editing and endogenous region sequencing)’을 개발했다.
돌연변이 검출 기술 ‘PEER-seq’에는 인공지능 기반의 최적화된 유전자편집 라이브러리를 통해 가능한 모든 형태의 단일염기서열 변이(Single nucleotide variant, SNV)를 도입했다. 추가적으로 도입된 변이를 정확히 탐지하기 위해 유전자 변이가 발생해도 단백질 아미노산 배열에는 변화가 생기지 않는 동의돌연변이를 추가로 도입했다.
이를 통해 PEER-seq 기술은 EGFR 유전자의 돌연변이 대부분이 관찰되는 티로신키나제 영역에서 알고리즘 기반의 프라임편집을 통해 모든 종양 변이 중 95% 이상을 검출할 수 있으며, 해당 돌연변이가 항암제 내성에 미치는 영향 정도를 평가할 수 있다. 유전자가위를 통해 세포의 수 변화를 간접적으로 추적했던 기존의 방식과 달리, 유전자편집이 이뤄진 유전체 내에서 직접 돌연변이의 약제 반응 정도를 확인하는 방식으로 더 높은 정확도의 기능평가를 진행할 수 있다.
연구팀은 PEER-seq 기술을 이용해 돌연변이가 발견된 세포주에 표적치료제 아파티닙과 오시머티닙을 투여한 후 2476개의 변이가 항암제에 저항성을 보이는지 평가했다. 또한 EGFR 유전자에서 가장 많이 발생하며 폐암 세포를 활성화하는 것으로 알려진 T790M 변이가 동반된 상태에서 다른 돌연변이가 유도된 ‘복합 변이’ 조합이 항암제 내성에 미치는 영향을 분석했다. 이를 통해 T790M이 동반된 상태에서만 알려져 있는 돌연변이들의 항암제 내성 여부가 T790M이 동반되는 않은 상태에서는 상당수 달라진다는 사실을 발견했다.
분석 결과, 2476개의 변이와 3가지의 약물 투여 조합에서 그동안 항암제에 대한 저항성 여부가 밝혀지지 않았던 46개 조합의 저항성 여부를 새롭게 발견했으며, 4270개 변이들의 약제 감수성을 확인할 수 있었다. 특히, 티로신키나제 영역에서 기존 진단키트로는 확인되지 않았던 K754Q, G930R, E931K 등과 같은 약제 저항성을 보이는 새로운 변이들도 발굴됐다.
또한 연구팀은 이번 연구를 통해 확인된 변이들이 항암제에 대해 감수성과 저항성을 보이는 특징이 기존 보고와 일치하는지 검증했다. 그 결과, 아파티닙과 오시머티닙 두 개의 약제 및 T790M 변이에 따른 63개의 약제-변이 조합 중 약 59개의 조합에서 기존 보고와 일치하는 결과를 확인하며 PEER-seq 기술의 높은 정확성을 입증했다.
김형범 교수는 “이번 연구로 개발된 PEER-seq 기술을 통해 많은 수의 돌연변이들의 약물 저항성을 높은 정확도로 한번에 분석할 수 있게 됐다”면서 “이 기술은 폐암 치료뿐 아니라 다른 암종에서도 다양한 항암제 및 변이 조합을 평가하는데 활용할 수 있어, 신약개발, 환자 맞춤형 치료 플랫폼 구축 등 정밀의학 실현에 있어 다양한 분야에서 활용할 수 있을 것”이라고 말했다.
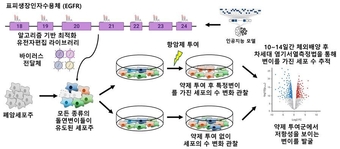
◈그림1 설명) PEER-seq 기술의 개괄. 표피생장인자수용체 티로신 키나제 영역에 알고리즘 기반 프라임편집을 통해 가능한 모든 종양 변이를 도입한 후 약제 투여를 통해 종양 변이가 항암제 내성에 얼마나 영향을 주는지 한번에 평가할 수 있는 기술.
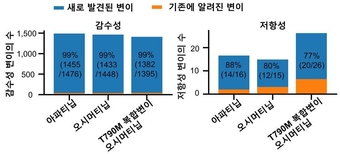
◈그림2 설명) PEER-seq 기술을 이용해 표피생장인자수용체 유전자에서 4270개 변이들의 약제 감수성과 그동안 항암제에 대한 저항성 여부가 밝혀지지 않았던 46개 조합의 저항성 여부를 새롭게 발견했다.